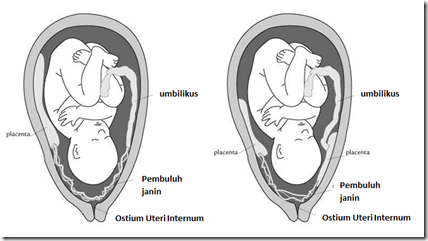
Amnion : selaput tipis pada hasil konsepsi yang terbentuk mulai hari ke 8 pasca konsepsi dan membentuk kantung kecil yang menutupi permukaan dorsal ‘embryonic disc”. Secara bertahap menyelubungi embrio yang tumbuh.
Cairan amnion : cairan yang berada dalam kavum amnion
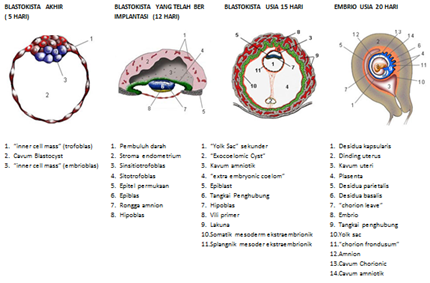
DINAMIKA CAIRAN AMNION
Pengaturan volume cairan amnion adalah proses dinamis yang mencerminkan keseimbangan antara produksi dan absorbsi cairan
PRODUKSI CAIRAN :
Pada usia < 8 minggu, cairan amnion dihasilkan oleh transudasi cairan melalui amnion dan kulit janin
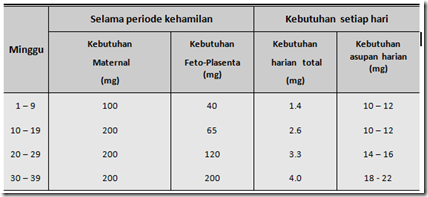
- Pada usia 8 minggu, janin mulai menghasilkan urine yang masuk kedalam rongga amnion. Urine janin secara cepat menjadi sumber utama produksi cairan amnion. Saat menjelang aterm, janin menghasilkan 800 – 1000 ml urine
- Paru janin menghasilkan sejumlah cairan ± 300 ml per hari saat aterm, namun sebagian besar ditelan sebelum masuk ruang amnion.
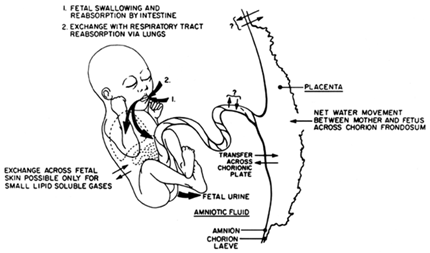
ABSORBSI CAIRAN :
- Pada usia kehamilan < 8 minggu, cairan amnion transudatif direabsorbsi secara pasif
- Pada usia kehamilan 8 minggu, janin mulai melakukan proses menelan. Proses ini secara cepat akan menjadi mekanisme utama absorbsi cairan amnion. Menjelang aterm, melalui proses menelan terjadi absorbsi cairan sebesar 500 – 100 mL per hari
- Absorbsi cairan amnion dalam jumlah sedikit juga terjadi melalui selaput amnion dan masuk kedalam aliran darah janin. Menjelang aterm , jalur ini melakukan absorbsi sebesar 250 ml.
- Sejumlah kecil cairan amnion melintas membran amnion dan masuk ke aliran darah ibu sebesar 10 ml per hari pada usia kehamilan menjelang aterm.
PERUBAHAN VOLUME CAIRAN AMNION SELAMA KEHAMILAN : Pada usia kehamilan 34 minggu, volume cairan amnion mencapai maksmial ( 750 -800 mL) dan setelah itu akan menurun sehingga pada usia kehamilan 40 minggu, volume cairan amnion ± 600 ml. Dan melewati usia 40 minggu, jumlah cairan amnion akan terus menurun.
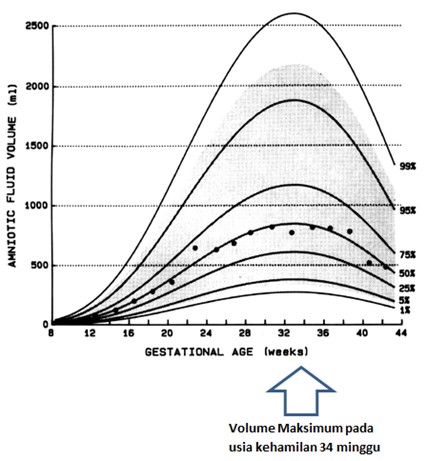
FUNGSI dan PERANAN CAIRAN AMNION
- Sebagai pelindung bagi janin terhadap trauma darim luar
- Melindungi talipusat dari tekanan
- Memungkinkan pergerakan janin secara bebas sehingga mendukung perkembangan sistem muskuloskeletal janin
- Berperan dalam perkembangan paru janin
- Melumasi kulit janin
- Mencegah korioamnionitis pada ibu dan infeksi janin melalui sifat bakteriostatik
- Membantu mengendalikan suhu tubuh janin
 Pemeriksaan dengan ultrasonografi adalah metode akurat untuk memperkirakan volume cairan amnion dibandingkan pengukuran tinggi fundus uteri .
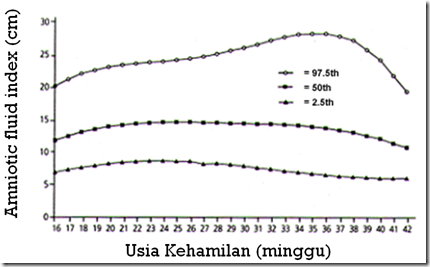
Pemeriksaan dengan ultrasonografi adalah metode akurat untuk memperkirakan volume cairan amnion dibandingkan pengukuran tinggi fundus uteri . Penentuan AFI – amniotic fluid index adalah metode semikuantitatif untuk memperkirakan volume cairan amnion.

AFI adalah jumlah dari kantung amnion vertikal maksimum dalam cm pada masing-masing empat kuadran uterus. AFI normal pada usia kehamilan lebih dari 20 minggu : 5 – 20 cm
ARTI KLINIK VOLUME CAIRAN AMNION Volume cairan amnion merupakan penanda kesehatan janin
- Volume cairan amnion normal menunjukkan bahwa perfusi uteroplasenta dalam keadaan memadai.
- Jumlah volume cairan amnuion abnormal berkaitan dengan “outcome”perinatal yang buruk
OLIGOHIDRAMNION
Batasan: jumlah cairan amnion yang kurang dari normal (kurang dari 300 ml) Angka kejadian: 5 – 8% kehamilan
Diagnosis :
- Kecurigaan terjadinya oligohidramnion bila tinggi fundus uteri lebih rendah dari yang diharapkan
- Ultrasonografi :
- Jumlah cairan amnion < 300 ml
- Ukuran kantung amnion vertikal ≥ 2 cm tidak ada
- AFI < 95 persentile untuk usia kehamilan tertentu
- Pada kehamilan aterm AFI < 5 cm
- Jumlah cairan amnion < 300 ml
- ABSORBSI KURANG atau KEHILANGAN CAIRAN MENINGKAT
- Ketuban Pecah Dini (50% kasus oligohidramnion)
- PENURUNAN PRODUKSI AMNION
- Kelainan kongenital ginjal (agenesis ginjal, displasia ginjal) dan paparan terhadap ACE inhibitor yang akan menurunkan output ginal janin
- Obstruksi orifisium urethra eksterna janin
- Insufisiensi uteroplasenta (solusio plasenta, preeklampsia, sindroma postmaturitas) menurunkan perfusi ginjal dan produksi uribne
- Infeksi kongenital – Defek jantung janin – NTD’s, sindroma twin to twin tranfusion,efek obat NSAID.
- Pilihan terapi pada masa antepartum sangat teerbatas, kecuali bila ditemukan defek struktural yang mengindikasikan untuk dilakukan pembedahan janin intrauterin
- Penentuan saat persalinan tergantung pada usia kehamilan – etiologi dan kesehatan janin.
- Selama proses persalinan, diberikan infus larutran kristaloid kedalam cavum amnion agar dapat
- Memperbaiki pola denyut jantung janin
- Menurunkan kejadian bedah SC
- Meminimalisir resiko sindroma aspirasi mekonium
- Memperbaiki pola denyut jantung janin
PROGNOSIS :
Oligohidramnion berkaitan dengan morbiditas dan mortalitas pada semua usia kehamilan
KOMPLIKASI:
- Amniotic Band Syndrome menyebabkan deformitas janin (amputasi atau deformitas muskuloskeletal)) a.l Clubfoot atau sindroma Potter

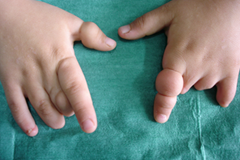

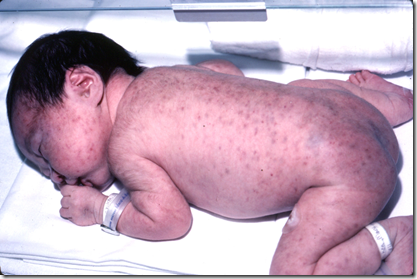
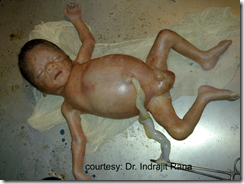
SINDROMA POTTER :
Sindroma Potter dapat berbentuk “clubbed feet”, Hipoplasia Pulmonal dan kelainan kranium yang terkait dengan oligohidramnion
POLIHIDRAMNION
Batasan: Jumlah cairan amnion lebih dari normal
Angka Kejadian: 0.5 – 1.5% seluruh kehamilan
Diagnosis:
- Kecurigaan terjadinya polihidramnion ditegakkan bila tinggi fundus uteri lebih dari yang diharapkan untuk usia kehamilan tertentu
- Ultrasonografi :
- volume air ketuban > 2 liter
- Kantung vertikal tungal > 10 cm
- AFI > 20 cm pada kehamilan aterm atau > 95 persentil untuk usia kehamilan tertentu
- Idiopatik (50 – 60% kasus)
- Penyebab maternal :
- isoimunisasi yang menyebabkan hidrop fetalis imune
- Diabetes Melitus
- Penyebab janin (10 – 15%):
- Hidrop fetalis non imune
- Defek jantung
- Kehamilan kembar
- Kelainan anatomis : obstruksi saluran intestin, deformitas paru, gangguan proses menelan (akalasia, obstruksi esopagus, fistula trakeoesopagus,kelainan SP
- Diabetes insipidus
- Penyebab plasenta (jarang) : korioangioma plasta
PENATALAKSANAAN
- Pilihan penatalaksanaan antepartum amat terbatas.
- Obat NSAID menyebabkan penurunan produksi urine janin namun dapat menyebabkan penutupan dini duktus arteriosus Bottali
- Amniosentesis memberikan hasil yang sementara
- Pada saat intrapartum, amniotomi terkendali dapat menurunkan angka kejdian dekompresi mendadak (solusio plasenta, prolapsus talipusat)
- Regangan rahim berlebihan dapat menyebabkan dispnea – edema tungkai bawah – edema vulva
- Selama persalinan, hidramnion dapat menyebabkan :
- Kelainan letak,
- Gangguan proses persalinan atau
- Perdarahan pasca salin.